열-탄소성 고체 거동의 지배 방정식에 대한 고찰
이번 게시물에서는 기하적 선형 범위 내에서 열-탄소성 거동을 보이는 고체를 묘사하기 위한 변수들과 기본 가정을 설명하고 힘의 평형 방정식과 에너지 평형 방정식의 유도, 그리고 최종적으로 열역학 제 2법칙의 결과로 얻게 되는 구성 방정식과 소성 변형에 대하여 고찰합니다.
열-탄소성 고체 거동, 열변형 해석
쉽게 이해하기👇
목차
1. 서론
2. 기본 가정
3. 평형 방정식
4. 열역학 제 2 법칙의 결과
5. 결론과 예제
1. 서론
일반적으로 탄소성(elasto-plasticity) 모델에 가장 적합한 재료는 금속이다. 금속 재료는 물성에 대한 모델이 비교적 정확하고 균질(homogeneous)하면서 등방성(isotropy) 구성을 보이는 경우가 많아서 이상적인 물성 모델링에 근접한 거동을 보인다. 그림 1은 표면에서 외력(표면력)을 받고 내부에서 체력( )을 받는 탄소성 고체를 나타낸 것이다.
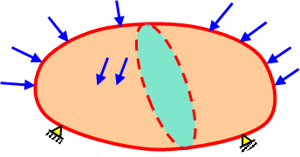
그림 1: 힘을 받는 탄소성 고체
이러한 탄소성 재료의 한 가지 취약점은 열에 약하다는 것이다. 상온에서의 거동과 비교하면, 온도가 상승할 때 금속 재료의 강성 (stiffness)과 강도(strength)가 계속 약해지는 경향이 있다. 이러한 거동을 묘사하기 위하여 많은 모델들이 개발되어 왔으며, 여기에서는 가장 기본적인 가정에서 시작하여 선형 열-탄소성 모델을 유도하는 과정을 설명하고자 한다.
2. 기본 가정
선형 해석에서 사용하는 탄소성 금속 모델의 경우 응력은 탄성 변형율의 함수이다. 즉,
σ = σ(ε^e) (1)
이고 여기서 ε^e은 탄성 변형율 텐서로 소성 변형율 텐서 ε^p와는
ε = ε^e + ε^p (2)
의 관계를 가진다.
열-탄소성 모델의 경우 다음과 같이 절대 온도 T에 대한 고려가 들어가는 것이 자연스럽다.
σ = σ(ε^e , T) (3)
위의 두 함수는 고체 영역의 모든 곳에서 각 변수에 대해 편미분이 가능하다고 가정한다.
3. 평형 방정식
탄소성 고체의 문제에서 고려해야 하는 평형 방정식은 힘의 평형 방정식이다. 즉, 정역학에서 선형 운동량 평형 방정식(balance of linear momentum)은 다음과 같이 표현된다.
∇⋅σ + b = 0 (4)
앞에서 나온 바와 같이 b는 체력(body force)을 나타낸다.
열-탄소성 고체의 문제에서는 에너지 평형 방정식이 추가로 요구된다.
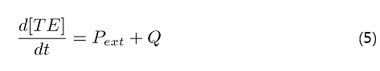
위 식에서 는 시스템이 가지고 있는 전체 에너지(total energy)로, 열 에너지와 탄성 에너지를 포함하는 내부 에너지 함수 E(internal energy)와 운동 에너지 K(kinetic energy)의 합으로 나타낼 수 있다. P_ext는 외부로부터 공급 받는 일률(power)이고, 는 시간 당 시스템에 입력되는 열 에너지(heat rate)이다. 즉, 시스템의 에너지 변화 속도는 외부로부터 입력 받는 에너지의 속도와 같다.
전체 영역의 운동 에너지 K는 속도 벡터 v 와 밀도 ρ를 사용하여 다음 식으로 나타낼 수 있다.
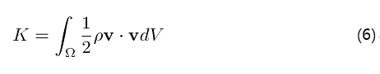
일률은 체력 "b" 와 표면 응력 "t" 에 대하여
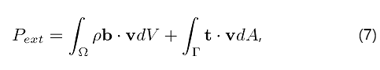
열에너지 입력은 내부 열원 r에 대하여
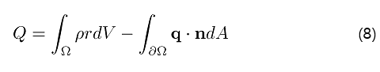
로 나타나며 q는 표면에서 바깥 방향으로 열의 흐름(heat flux)을 나타내는 벡터이다. 전체 시스템의 내부 에너지는 단위 부피 당 내부 에너지 함수 e로 나타낼 수 있다. 즉,

이제 식(7)로부터 다음 식을 유도할 수 있다.
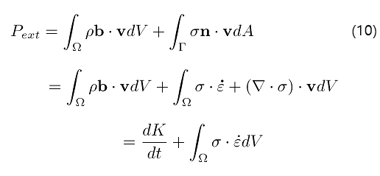
위 결과들을 식 (5)에 적용하면 전체 영역에 대한 에너지 평형식을 얻는다.
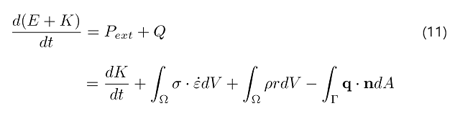
위 식을 전부 체적분으로 수정하면 최종 에너지 평형 방정식을 얻는다:
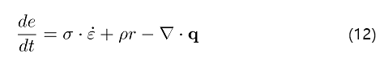
한편, e=e ̃(ε^e,η)를 이용하면,
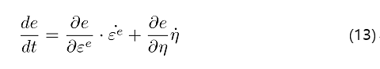
두 식을 연립하면 엔트로피와 소성 변형율의 시간 변화율을 포함한 에너지 평형 방정식을 얻는다.
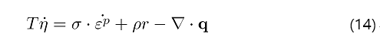
4. 열역학 제 2 법칙의 결과
열역학 제 2 법칙은 에너지의 이동 방향을 정의해주는 정리이다. 여기에서는 2법칙의 핵심이 되는 엔트로피(entropy)에 대한 설명은 생략하고 그 상태 함수(state function)의 존재를 가정하는 것으로 시작한다.
주어진 닫힌 영역 에 대하여 단위 부피 당 엔트로피 함수 η가 존재하여 전체 엔트로피 S는 다음과 같이 쓸 수 있다.

응력 함수 σ와 마찬가지로 다른 함수들도 변형과 온도, 엔트로피의 함수로 정의할 수 있다. 따라서,
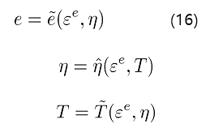
이제 위에서 정의한 함수들을 사용하여 열역학 제 2 법칙을 정의한다.

위 부등식은 열역학 제 2 법칙을 나타내는 여러 부등식 중의 하나인 Clausius-Duhem 부등식이다. 여기서 γ^_int은 내부 엔트로피 증가율로 다음과 같이 정의된다.

γ^_ext는 외부 엔트로피 입력율로, 외부 에너지 입력율을 절대 온도로 나눈 형태로 정의된다.
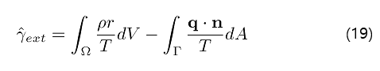
따라서 제 2 법칙이 의미하는 것은 외부에서 들어오는 엔트로피의 증가율보다 내부 엔트로피의 증가율이 더 빠르다는 것이다. 이제 식(15)와 (16)을 식(14)에 대입하여 정리하면 영역 내 모든 곳에서 만족해야 하는 부등식을 얻는다.
😥 미리 보기는 여기까지!
내용을 이어서 보고 싶다면,
아래 정보를 입력해 주세요.







-png.png?width=400&name=%EB%B0%98%EB%94%94%ED%86%B5_CAE-Expert_%ED%91%9C%EC%A7%80-002%20(3)-png.png)










